Crinetics Pharmaceuticals社の経口の先端巨大症(末端肥大症)薬paltusotine(パルツソチン)のPh3試験PATHFNDR-1が主要目標も副次目標も達成しました。
試験にはソマトスタチンの類い(octreotideかlanreotideのどちらかのデポ剤)を注射していてIGF-1量が正常範囲上限以内の先端巨大症患者58人が参加しました。
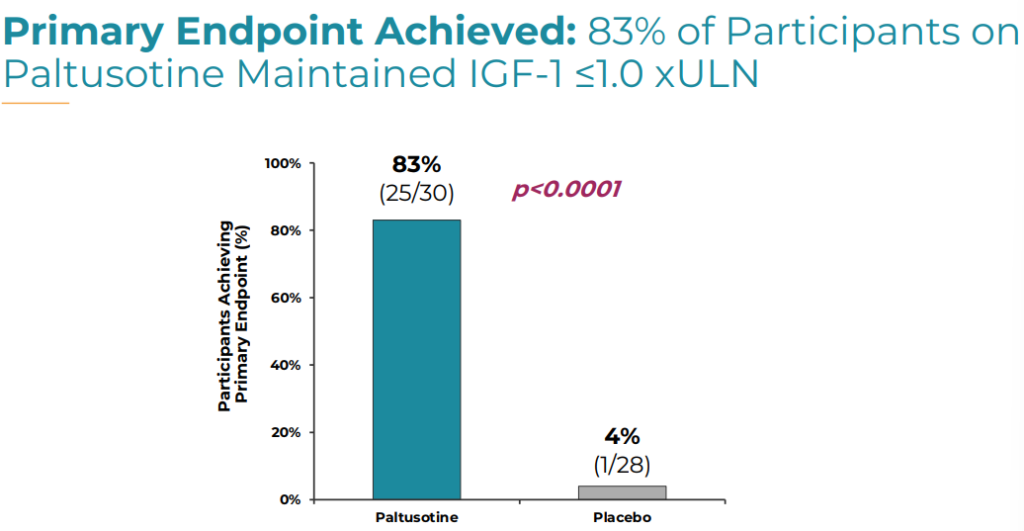
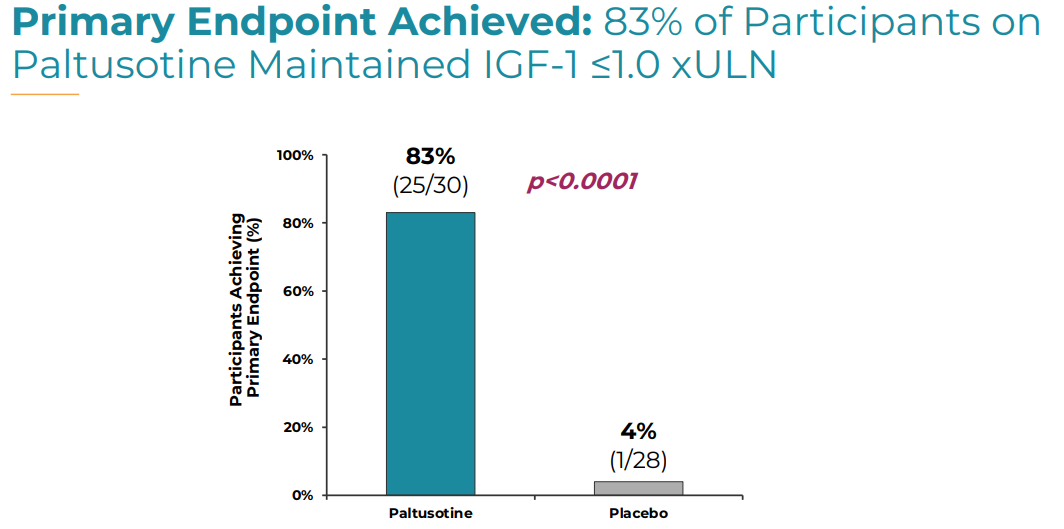
36週間の1日1回paltusotine経口服用に割り振られた30人の83%(25人)がIGF-1量正常範囲上限以内を保ちました。一方、プラセボ群28人でIGF-1量正常範囲上限以内を保った患者は殆どおらず1人のみ(4%)でした。
paltusotineはソマトスタチン受容体2型(SST2)を活性化します。
薬を使っていないか未治療でIGF-1値が高い患者へのpaltusotineのもう1つのPh3試験PATHFNDR-2が進行中で、その結果一揃いが来年2024年1Qに判明します。PATHFNDR-2が成功したらCrinetics社は同剤を来年中に米国FDAに承認申請します。
TOPLINE RESULTS FROM PALTUSOTINE PHASE 3 PATHFNDR-1 STUDY / Crinetics
www.crinetics.com/wp-content/uploads/2023/09/20230911-Phase-3-PATHFNDR-1-Topline-Results.pdf
Crinetics soars on positive acromegaly study of oral drug / FirstWord
www.firstwordpharma.com/story/5779371


コメント